Phản ứng thế là một loại phản ứng hoá học có vai trò quan trọng trong nghiên cứu cũng như trong đời sống. Vậy phản ứng thế là gì? Phản ứng thế có những đặc điểm như thế nào? Hãy cùng tìm hiểu về loại phản ứng này trong bài viết sau đây nhé.
Contents
Tìm hiểu khái niệm phản ứng thế
Phản ứng thế được định nghĩa là phản ứng trong đó nhóm chức của một hợp chất hóa học được thay thế bằng một nhóm khác. Nó cũng có thể là phản ứng liên quan đến việc thay thế một nguyên tử hoặc một phân tử của hợp chất bằng một nguyên tử hoặc phân tử khác.

Điều kiện của phản ứng thế
Để phản ứng thế xảy ra thì cần có một số điều kiện nhất định như sau:
- Duy trì nhiệt độ phản ứng bằng nhiệt độ phòng.
- Các bazơ trong phản ứng nếu mạnh như NaOH thì nó phải ở dạng loãng. Giả sử nếu bazơ có nồng độ cao hơn thì có khả năng xảy ra quá trình khử halogen.
- Các chất tham gia phản ứng phải ở dạng dung dịch.
Ví dụ về phản ứng thế
Một ví dụ về phản ứng thế là khi CH3Cl phản ứng với ion hydroxyl (OH-), nó sẽ dẫn đến sự hình thành phân tử ban đầu gọi là metanol với ion hydroxyl đó. Phản ứng được mô tả với phương trình:
CH3Cl + (OH− ) → CH3OH( metanol) + Cl–
Một ví dụ nữa là phản ứng của Ethanol với hydro iodua tạo thành iodoethane cùng với nước. Phản ứng được mô tả với phương trình như sau:
CH3CH2OH + HI → CH3CH2I + H2O
Phân loại phản ứng thế
Phản ứng thế có hai loại là phản ứng nucleophilic và phản ứng điện di. Hai loại phản ứng này chủ yếu khác nhau ở loại nguyên tử được gắn vào phân tử ban đầu của nó. Trong các phản ứng nucleophin, nguyên tử là loại giàu điện tử, trong khi đó, trong phản ứng điện di, nguyên tử là loại thiếu điện tử.
Phản ứng thế Nucleophilic
Nucleophiles là những chất hoá học ở dạng ion hoặc phân tử được gắn mạnh vào vùng mang điện tích dương. Các phân tử của chúng thường có nhiều ion âm. Các ví dụ phổ biến của nucleophile là các ion xyanua, nước, ion hydroxit và amoniac.
Phản ứng thế Nucleophilic trong hóa học hữu cơ là một loại phản ứng trong đó một nucleophile được gắn vào các nguyên tử hoặc phân tử tích điện dương của chất khác.
Một ví dụ điển hình về phản ứng thế Nucleophile là quá trình thủy phân alkyl bromide (R-Br), trong các điều kiện cơ bản, trong đó Nucleophilic bazơ OH – , nhóm rời đi là Br – . Phản ứng hoá học của nó có dạng:
R-Br + OH − → R-OH + Br −
Các phản ứng nucleophin cũng quan trọng trong lĩnh vực hóa học hữu cơ và những phản ứng này phổ biến là phản ứng thế vị trí của một nguyên tử cacbon trong hợp chất cacbon béo bão hòa.
Phản ứng thế điện di
Phản ứng thế điện di liên quan đến các điện di. Điện di là những chất tặng một cặp electron trong quá trình hình thành liên kết cộng hóa trị. Các phản ứng điện di xảy ra chủ yếu với các hợp chất thơm. Các hợp chất này có lượng electron dư thừa có thể được chia sẻ với tất cả các chất của phản ứng.
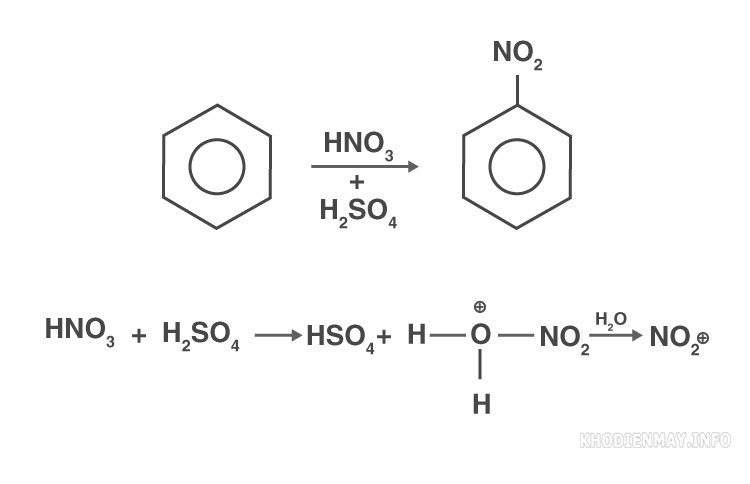
Các phản ứng thế điện di về cơ bản được định nghĩa là những phản ứng hóa học trong đó chất điện di thay thế nhóm chức trong hợp chất chứ không phải nguyên tử hydro. Một số ví dụ về các loại điện di bao gồm ion hydronium (H3O+ ), halogenua của hydro như HCl, HBr, HI, sulfur trioxide (SO3 ), ion nitronium (NO2 + )…
Có 2 loại phản ứng thế điện di là phản ứng thế điện di thơm và phản ứng thế điện di aliphatic.
Phản ứng thế điện di thơm
Trong kiểu phản ứng thế điện di này, một nguyên tử gắn vào vòng thơm, chủ yếu là hydro được thay thế bằng một điện di. Các phản ứng có thể xảy ra là halogen hóa thơm, phản ứng Friedel-Crafts alkyl hóa, nitrat hóa thơm, sulfo hóa và acyl hóa thơm.
Phản ứng thế điện di aliphatic
Trong loại phản ứng thế điện di này, một chất điện di sẽ thay thế cho một nhóm chức năng.
Phản ứng thế của một số nhóm chất hoá học
Trong hoá học, có một vài nhóm phân tử hoá học đặc trưng bởi phản ứng thế. Chúng ta hãy cùng tìm hiểu về các nhóm chất này ngay sau đây nhé.
Phản ứng thế của ankan
Ankan là một nhóm chất hiđrocacbon no mạch hở: CnH2n+2 (n ≥1). Phản ứng thế là đặc trưng của ankan vì phân tử ankan chỉ chứa liên kết đơn.
CnH2n+2 + xX2 → CnH2n+2-xXx + xHX
Về nguyên tắc, số nguyên tử H trong phân tử ankan có thể thay thế từ 1 đến hết.
Khả năng phản ứng giảm dần theo thứ tự F2 > Cl2 > Br2 > I2.
Thông thường, chúng ta không nhận được phản ứng đối với flo vì nó phản ứng mạnh và thường gây ra phản ứng hủy:
CnH2n+2 + (n+1)F2 → nC + (2n+2)HF
Ngoài ra khi ankan phản ứng với Iot thì phản ứng yếu, phản ứng với Clo thì cần điều kiện ánh sáng và phản ứng với Brom cần đun nóng.
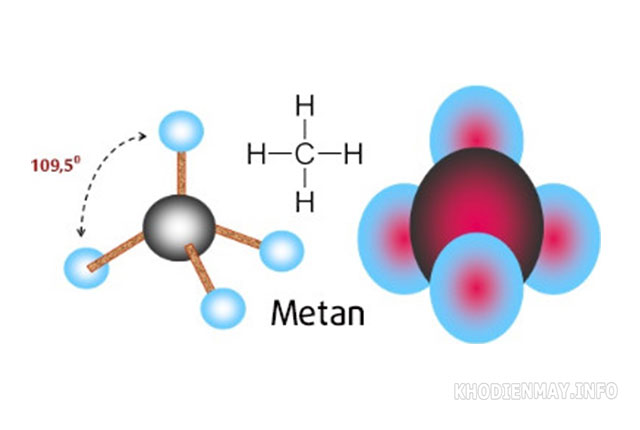
Phản ứng thế của metan
Metan là chất có công thức hoá học là CH4. Một tính chất hóa học quan trọng của metan đó là phản ứng thế với các halogen như clo, brom… Nó phản ứng với hơi nước để tạo ra hydro, phản ứng với oxy để bắt lửa và phân hủy khí metan để tạo ra acetylene C2H2.
Có thể bạn quan tâm:
Ví dụ: Phản ứng thế của metan thế H với halogen khi có ánh sáng:
Khi có ánh sáng hoặc nhiệt độ, halogen có thể thay thế mọi phân tử H trong phân tử metan để tạo thành dẫn xuất halogen.
CH3-H + X2 → hv/to CH3-X+ HX
Bài viết đã giới thiệu những thông tin cơ bản về phản ứng thế. Đây là kiến thức hóa học quan trọng mà bạn cần ghi nhớ. Hy vọng sau khi đọc xong bài viết bạn đã có thêm nhiều kiến thức về loại phản ứng hoá học này.

